

“醫(yī)療物資出口產(chǎn)地檢驗(yàn)”事件一波三折。海關(guān)最新消息指出,按照72號(hào)文件要求,對(duì)于53號(hào)公告規(guī)定的11類(19個(gè)商品編碼)出口法檢醫(yī)療物資,采取的是驗(yàn)證管理方式,意味著無需實(shí)施產(chǎn)地檢驗(yàn),報(bào)關(guān)時(shí)不需要出口電子底賬,企業(yè)正常申報(bào)報(bào)關(guān)單。
有業(yè)內(nèi)人士指出,雖然目前實(shí)際操作中,仍是按照之前的正常申報(bào),且不會(huì)被退單,但幾乎99%都會(huì)被查驗(yàn),出口通關(guān)審核趨嚴(yán)。
口罩等防疫物資資質(zhì)梳理,美國和歐洲當(dāng)?shù)刭Y質(zhì)要求各異
據(jù)賣家爆料稱:“自上周開始,歐洲ECM認(rèn)證機(jī)構(gòu)已經(jīng)停止接單,就連FDA也全面停止接單了。身邊已有同行口罩機(jī)都已準(zhǔn)備就緒,非要安裝好后再進(jìn)行申請(qǐng)認(rèn)證,奈何機(jī)器安裝到一半認(rèn)證通道卻關(guān)閉了,巧婦難為無米之炊。”
對(duì)此,深圳合眾商務(wù)咨詢有限公司副總經(jīng)理張劍表示,盡管當(dāng)前海關(guān)公告明確指出醫(yī)療物資出口無需實(shí)施產(chǎn)地檢驗(yàn),但出口企業(yè)切忌掉以輕心,不排除未來醫(yī)用口罩等防疫物資會(huì)被列為出口法檢的可能。因此,建議出口企業(yè)應(yīng)積極準(zhǔn)備法檢合規(guī)產(chǎn)品,對(duì)接合規(guī)且有資質(zhì)的廠家,如果是手頭仍有庫存的情況下,則盡快將產(chǎn)品發(fā)往海外才是明智之舉。
據(jù)介紹,從事口罩等防疫物資的出口企業(yè),應(yīng)在口岸報(bào)關(guān)前向生產(chǎn)地、組貨地海關(guān)提出申請(qǐng),且滿足產(chǎn)品生產(chǎn)和發(fā)貨地資質(zhì)要求,以及產(chǎn)品銷售地資質(zhì)要求。
1、產(chǎn)品的生產(chǎn)和發(fā)貨地資質(zhì)要求:主要包括海關(guān)出口、行業(yè)政府監(jiān)管,以及工廠出廠生產(chǎn)這三點(diǎn)。
以口罩出口為例,包括如下幾點(diǎn):
(1)生產(chǎn)廠家需要提供有第三方檢測(cè)機(jī)構(gòu)提供的口罩產(chǎn)品檢測(cè)報(bào)告;
(2)行業(yè)監(jiān)管要求,需要銷售口罩的公司具備醫(yī)療器械產(chǎn)品銷售資質(zhì),口罩等一般防疫物資需要申請(qǐng)國內(nèi)二類醫(yī)療備案許可資質(zhì);
(3)海關(guān)要求,銷售口罩的公司要具備貨物出口權(quán)資質(zhì)。
2、產(chǎn)品的銷售地資質(zhì)要求
其一、美國當(dāng)?shù)亍?/strong>
目前,美國當(dāng)?shù)氐男袠I(yè)監(jiān)管及海關(guān)監(jiān)管,需要對(duì)防疫物資具備FDA資質(zhì)認(rèn)證才可以進(jìn)口清關(guān)。
那么,美國FDA認(rèn)證需要具備哪些條件呢?目前,美國對(duì)口罩認(rèn)證分為兩種,一種是需要注冊(cè)一類FDA認(rèn)證的防護(hù)口罩;另一種是需要二類FDA認(rèn)證的醫(yī)用口罩。
張劍表示,通常情況下二類FDA認(rèn)證時(shí)間長達(dá)十個(gè)月,且注冊(cè)費(fèi)用昂貴接近20萬人民幣,國內(nèi)真正意義上申請(qǐng)二類FDA認(rèn)證的醫(yī)用口罩出口企業(yè)屈指可數(shù)。另有官網(wǎng)數(shù)據(jù)顯示,最近三年中國企業(yè)獲得美國FDA二類認(rèn)證的企業(yè)是個(gè)位數(shù)。
“目前大多數(shù)企業(yè)的做法是把防護(hù)口罩和符合醫(yī)用標(biāo)準(zhǔn)的醫(yī)用口罩都只能按照防護(hù)類口罩申請(qǐng)一類FDA認(rèn)證,這就導(dǎo)致KN95口罩(屬于醫(yī)用口罩)在清關(guān)時(shí)被抽查容易觸發(fā)潛在風(fēng)險(xiǎn)。口罩是醫(yī)用標(biāo)準(zhǔn)還是防護(hù)標(biāo)準(zhǔn),只能在國內(nèi)采購時(shí)與廠家或是供應(yīng)商確定好產(chǎn)品規(guī)格,目前大家的做法就是把防護(hù)口罩和醫(yī)用口罩都在FDA一類防護(hù)口罩申請(qǐng)認(rèn)證資質(zhì),現(xiàn)在國內(nèi)幾乎是找不到具備FDA二類認(rèn)證的工廠廠家。”他透露。
其二、歐洲當(dāng)?shù)亍?/strong>
歐洲口罩等防疫產(chǎn)品需要具備CE認(rèn)證,CE認(rèn)證對(duì)口罩也分為防護(hù)口罩和醫(yī)用口罩兩種。就目前來看,國內(nèi)的商家通常申請(qǐng)的大多數(shù)是CE防護(hù)口罩認(rèn)證資質(zhì),防護(hù)等級(jí)FFP2,執(zhí)行標(biāo)準(zhǔn)EN149-2009。
據(jù)張劍介紹,中國賣家申請(qǐng)CE認(rèn)證,需要具備在歐洲當(dāng)?shù)氐恼J(rèn)證機(jī)構(gòu)遞交認(rèn)證申請(qǐng),可以自由選擇認(rèn)證機(jī)構(gòu)。而如果在國內(nèi)申請(qǐng)CE認(rèn)證,只能通過當(dāng)?shù)貦C(jī)構(gòu)授權(quán)給國內(nèi)認(rèn)證機(jī)構(gòu)的機(jī)構(gòu)才可以申請(qǐng)成功。“目前尚無可定論哪家機(jī)構(gòu)的證書是真實(shí)有效,每一份CE證書會(huì)對(duì)應(yīng)一份產(chǎn)品檢測(cè)報(bào)告,沒有檢測(cè)報(bào)告的CE證書將面臨巨大的商業(yè)風(fēng)險(xiǎn)和法律風(fēng)險(xiǎn)。”
除此之外,針對(duì)CE在歐洲清關(guān)貨物被扣的問題。一位不具名的資深物流服務(wù)人士坦言,當(dāng)前跨境服務(wù)市場(chǎng)魚龍混雜,不排除會(huì)有部分不專業(yè)且不負(fù)責(zé)任的企業(yè)會(huì)把防護(hù)口罩申報(bào)和醫(yī)用口罩申報(bào)混為一談,打著口罩檢測(cè)報(bào)告名義進(jìn)行清關(guān),最終導(dǎo)致被海關(guān)查驗(yàn)扣貨。他強(qiáng)調(diào),“尤其是從事口罩等防疫物資的出口企業(yè),凡是提供有效的CE認(rèn)證,不要輕易在清關(guān)時(shí)申報(bào)高規(guī)格口罩標(biāo)準(zhǔn),確保口罩產(chǎn)品品質(zhì)有保障,才能大大降低產(chǎn)品被扣貨的幾率。”
海關(guān)53號(hào)文件“余震”,外貿(mào)B2B和跨境B2C如何對(duì)癥下藥?
“外貿(mào)B2B和跨境B2C對(duì)于醫(yī)用口罩等防疫物資出口具備資質(zhì)實(shí)際上大有不同,這往往也是出口企業(yè)容易忽視之處。”張劍分析道,一種是外貿(mào)B2B的企業(yè)通常都會(huì)有自己的進(jìn)出口權(quán)公司,具備貨物進(jìn)出口資質(zhì),公司的貨物出口是采用自己的進(jìn)出口權(quán)公司進(jìn)行出口報(bào)關(guān)及出口退稅;另一種跨境B2C賣家,大部分是不做出口退稅,貨物出口清關(guān)主要是外包交由專業(yè)FBA頭程公司一站式解決,支付相應(yīng)運(yùn)費(fèi)即可。僅有少數(shù)賣家會(huì)做小部分出口退稅,這類賣家中還有一部分是用物流公司的資質(zhì)做出口退稅的情況,實(shí)則擁有進(jìn)出口資質(zhì)的公司少之又少。
隨著海關(guān)53號(hào)文件出臺(tái),不同類型出口企業(yè)面臨的難題各異。“一方面,對(duì)于已經(jīng)擁有貨物進(jìn)出口資質(zhì)的外貿(mào)B2B企業(yè),只需要在原來的基礎(chǔ)上,增加海關(guān)產(chǎn)品檢驗(yàn)檢疫資質(zhì)備案申請(qǐng),申請(qǐng)國內(nèi)二類醫(yī)療備案銷售許可資質(zhì)。上游供應(yīng)商提供第三方權(quán)威機(jī)構(gòu)出具的產(chǎn)品檢測(cè)報(bào)告,只要產(chǎn)品品質(zhì)符合相關(guān)要求即可符合海關(guān)最新的出口條件了;另一方面,大多數(shù)跨境B2C賣家不具備貨物進(jìn)出口權(quán)的資質(zhì),有的賣家用自己不具備貨物進(jìn)出口權(quán)的公司申請(qǐng)了國內(nèi)二類醫(yī)療備案許可。”他說。
卓志跨境電商總裁李金玲也針對(duì)醫(yī)療物資出口,通關(guān)單填報(bào)的注意事項(xiàng)提出如下幾點(diǎn):
1、領(lǐng)證機(jī)關(guān):企業(yè)申請(qǐng)電子底賬的屬地海關(guān)代碼;
2、品名,商品編碼,品牌,型號(hào),成交單位,成交數(shù)量,貨物總值保持與報(bào)關(guān)資料一致;
3、通關(guān)單信息中的境內(nèi)發(fā)貨人、運(yùn)抵國、項(xiàng)數(shù)、次序與報(bào)關(guān)信息確保一致;
4、出口貨物報(bào)關(guān)單上的“申報(bào)日期”必須在出境貨物通關(guān)單的有效期內(nèi)。需要注意的是,目前申報(bào)系統(tǒng)已升級(jí),通關(guān)單數(shù)量和項(xiàng)數(shù)要與報(bào)關(guān)單一致,否則將無法通過審核。
根據(jù)商務(wù)部、海關(guān)總署、國家藥品監(jiān)督管理局發(fā)布的2020年第5號(hào)最新公告指出,自4月1日起,出口新型冠狀病毒檢測(cè)試劑、醫(yī)用口罩、醫(yī)用防護(hù)服、呼吸機(jī)、紅外體溫計(jì)的企業(yè)向海關(guān)報(bào)關(guān)時(shí),須提供書面或電子聲明(模版如下圖所示),承諾出口產(chǎn)品已取得中國醫(yī)療器械產(chǎn)品注冊(cè)證書,從而符合進(jìn)口國(地區(qū))的質(zhì)量標(biāo)準(zhǔn)要求。海關(guān)將憑藥品監(jiān)督管理部門批準(zhǔn)的醫(yī)療器械產(chǎn)品注冊(cè)證書驗(yàn)放。
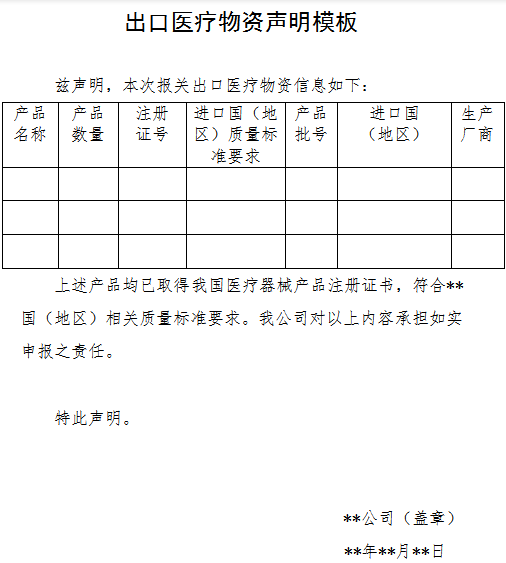
(出口醫(yī)療物資聲明模版截圖)
最后,張劍總結(jié)道:“不論口罩是否需要檢驗(yàn),這對(duì)于從事口罩等防疫物資的企業(yè)來說,當(dāng)務(wù)之急是盡快有一家自己的公司,具備貨物進(jìn)出口權(quán)資質(zhì),獲得海關(guān)檢驗(yàn)檢疫備案許可,申請(qǐng)國內(nèi)二類醫(yī)療器械銷售許可。與此同時(shí),出口產(chǎn)品品質(zhì)應(yīng)當(dāng)符合相關(guān)行業(yè)標(biāo)準(zhǔn),產(chǎn)品具備國內(nèi)第三方權(quán)威檢測(cè)機(jī)構(gòu)出具的產(chǎn)品檢測(cè)報(bào)告,未雨綢繆做好萬全準(zhǔn)備,以不變應(yīng)萬變。”
(文/雨果網(wǎng) 陳林)
【特別聲明】未經(jīng)許可同意,任何個(gè)人或組織不得復(fù)制、轉(zhuǎn)載、或以其他方式使用本網(wǎng)站內(nèi)容。轉(zhuǎn)載請(qǐng)聯(lián)系:editor@cifnews.com
相關(guān)閱讀推薦:
①口罩列為出口法檢!專家解讀海關(guān)53號(hào)文件背后的“故事”
②海關(guān)最新消息:醫(yī)療物資出口無需實(shí)施產(chǎn)地檢驗(yàn)!



